【技术速递】Maurice CE-SDS快速表征LVV慢病毒载体
免疫疗法正在发展成为一种可用于多种恶性肿瘤的有效且侵入性较小的治疗方法。慢病毒载体(Lentiviral vectors,LVV) 因其能够稳定地整合相对较大的外源DNA,并且有效地转导分裂细胞和非分裂细胞,已成为免疫治疗领域中具有广泛应用前景的明星载体工具1,2。迄今为止,已有超过315种基于LVV的基因疗法正在临床试验中3。
临床应用对慢病毒载体具有较高的质量要求,如何确保产品的安全性和有效性始终是质量控制的核心。传统的纯度检测方法SDS-PAGE是一种手动且劳动密集型的方法,通常还伴随着重现性差的问题,而ELISA方法也存在高估感染性病毒滴度的问题。因此为了加快LVV产品的开发,迫切需要更加稳定、准确及可靠的表征分析工具保证其安全性及有效性。
Maurice是ProteinSimple开发的一款完全集成的毛细管电泳(CE)分析平台,兼具分析蛋白质大小异质性的CE-SDS和蛋白质电荷异质性的icIEF。免组装卡盒设计使得两种应用切换非常方便。对于高通量应用,可使用仅需5.5分钟/针的Turbo CE-SDS™卡盒即可获得CE-SDS数据,如果需要进一步表征,则使用25分钟/针的CE-SDS PLUS卡盒即可获得可重复的高质量数据,不同实验室之间可进行无缝方法转移。Maurice CE-SDS能同时表征LVV三大关键质量属性(CQAs):纯度、滴度和鉴别。

唯一一款iCIEF和CE-SDS双药典设备
Maurice CE-SDS PLUS分析LVV纯度的日内重复性
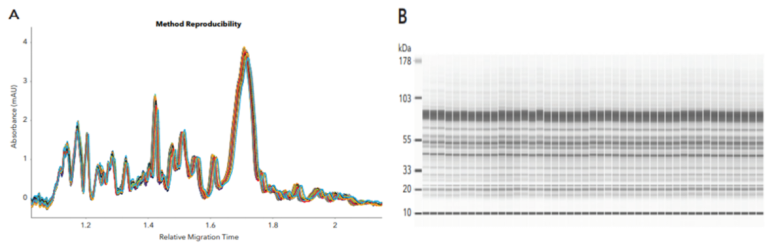
图1:45针样品连续进样的电泳叠图(A)及模拟胶图(B)
为了评估CE-SDS PLUS方法的日内重复性,单个LVV样品连续进样45针,结果显示尽管LVV结构复杂,但显示出出色的重现性,平均总峰面积的RSD值仅为2.91%(图1A),并且Compass for iCE软件还可生成模拟胶图(图1B),有利于将大型数据集进行可视化分析。
Maurice CE-SDS PLUS分析LVV纯度的日间重复性
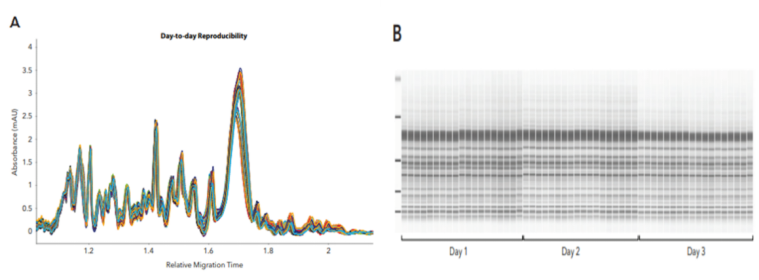
图2:连续3天3个LVV样品重复进样6针的电泳叠图(A)及模拟胶图(B)
为了评估CE-SDS PLUS方法的日间重复性,连续3天每天制备3个不同的LVV样本,每个样本在Maurice上运行6个重复,共进样54针。所有54个样本的数据重现性结果显示出卓越的重现性,平均总峰面积的RSD值为3.38%(图2A)。
LVVs的线性、LOD和LOQ测定
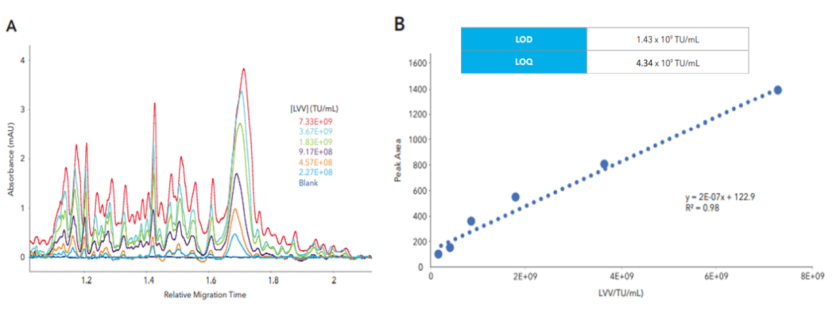
图3:LVVs的线性(A)、LOD和LOQ测定(B)
为了确定该方法的线性和检测限,对LVV样品进行连续稀释进样。结果显示峰面积随着样品浓度的增加而增加(图3A),且呈线性相关,R2值为0.98(图3B)。并使用该稀释方法确定了检出限LOD和定量限LOQ分别是1.43x109TU/mL和4.34x109TU/mL,LOD的计算方法是将峰高的标准差除以校准曲线的斜率,LOQ是使用峰高标准差的10倍除以斜率。
LVVs病毒滴度测定
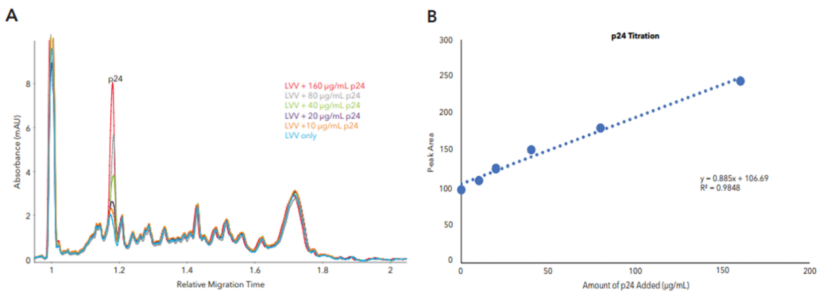
图4:p24加标测定LVV病毒滴度
p24蛋白测定是确定LVV病毒滴度的主要方法之一,在本研究中,在LVV中加入不同浓度的p24,并进行CE-SDS分析,结果显示随着p24浓度的增加,p24峰值强度明显增加(图4A)。利用峰面积对p24浓度进行滴定曲线绘制,发现峰面积与p24浓度呈正相关,R2值为0.9848 (图4B)。与《自然》杂志发表的105TU LVV中检测到1 ng p24相比,本研究中109TU/mL的LVV中能检测到的p24浓度约为8.5µg/mL,在理论值的15%以内。
LVVs的鉴别

图5:不同LVV颗粒的鉴别
LVV载体的鉴别对于确保LVV一致性至关重要,Maurice CE-SDS可快速的对不同的LVV载体进行鉴别,区分出不同LVV的相似点和不同点(5A),为相应质量标准的建立提供有力依据。
总结
LVV载体的鉴别对于确保LVV一致性至关重要,Maurice CE-SDS可快速的对不同的LVV载体进行鉴别,区分出不同LVV的相似点和不同点(5A),为相应质量标准的建立提供有力依据。

参考文献
1. Milone, M. C., & O’Doherty, U. (2018). Clinical use of lentiviral vectors. Leukemia, 32(7), 1529–1541. https://doi.org/10.1038/s41375- 018-0106-0
2. White, M., Whittaker, R., Gándara, C., & Stoll, E. A. (2017). A Guide to Approaching Regulatory Considerations for Lentiviral-Mediated Gene Therapies. Human gene therapy methods, 28(4), 163–176. https://doi.org/10.1089/hgtb.2017.096
3. Bulcha, J.T., Wang, Y., Ma, H. et al (2021). Viral vector platforms within the gene therapy landscape. Sig Transduct Target Ther 6, 53 https://doi.org/10.1038/s41392-021-00487-6
4. Tiscornia, G., Singer, O. & Verma, I. Production and purification of lentiviral vectors. Nat Protoc 1, 241–245 (2006). https://doi.org/10.1038/nprot.2006.37
5. Lentiviral Vector Characterization Made Easy with Maurice CE-SDS。Application Note